宫颈癌患者的福音:武汉卡必斯全球首个新药获
日期:2025-10-14 12:14 浏览:
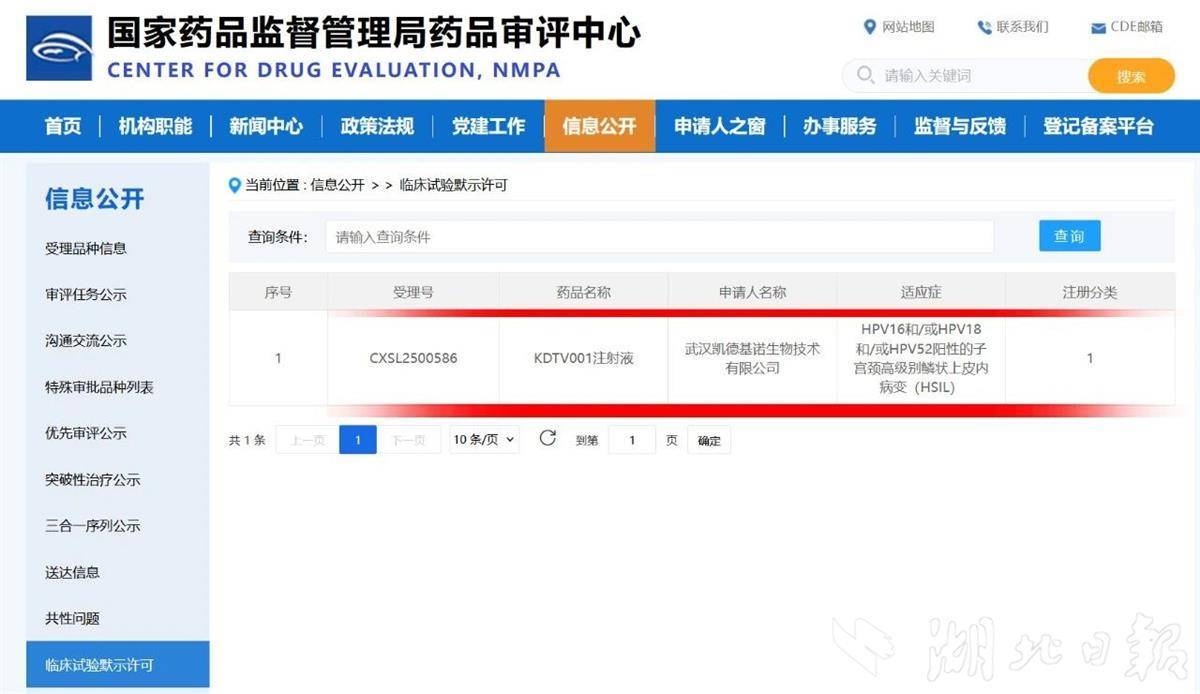
湖北日报讯(记者张珍珍)10月13日,武汉卡德维斯生物科技有限公司(以下简称“卡德维斯”)宣布,其自主研发的一类创新注射剂新药KDTV001的临床试验申请获中国国家药品监督管理局批准,取得全球首创结果。同时,该药于9月26日向美国食品药品监督管理局(FDA)提交临床试验申请,进入审评阶段。 KDTV001注射液在中国获批,是主动免疫治疗的生物药。最初将进行I期临床试验,以评估注射液在患有HPV 16/18/52阳性的高级别宫颈鳞状上皮内病变的成年女性患者中的安全性、耐受性、免疫原性和初步疗效。宫颈癌是一种恶性肿瘤,严重威胁全世界女性的健康,在日本发病率居第二位。这是 e预计到2020年,全球将有604,000名女性被诊断患有宫颈癌,约342,000名女性将死于这种癌症。世界卫生组织的加速消除宫颈癌全球战略指出,90% 被诊断患有宫颈癌的女性需要治疗。持续的高危人乳头瘤病毒(HPV)感染是宫颈癌和癌前病变的主要原因。特别值得关注的是最重要的癌前阶段、宫颈高级鳞状上皮内病变 (CIN2/3) 的临床风险。权威研究数据证实,未经治疗的CIN3患者中有30%~50%会在30年内发展为宫颈癌,且随着病程延长,这种风险可能进一步累积,凸显了早期有效干预宫颈重度鳞状上皮内病变的紧迫性。 KDTV001注射液主要针对晚期实体瘤、肿瘤等适应症。早期非侵袭性肿瘤,以及HPV感染引起的宫颈高级鳞状上皮内病变。该注射液由凯德维斯旗下武汉凯德金果生物科技有限公司研发,负责创新生物医药产品的研发。卡德威斯是与华中科技大学同济医学院附属同济医院及马丁学术成员团队合作创立的一家新型国家专业“小巨人”公司。公司已申请专利51项,其中发明专利48项,实用新型专利3项。此外,我们还建立了完整的活病毒载体基因治疗药物平台,从研发到生产的高效率,保证了药品的安全性、有效性和质量可控。 2023年,公司基因治疗药物KD01重组溶瘤病毒获得国家药品监督管理局批准并进入I期临床试验。
 湖北日报讯(记者张珍珍)10月13日,武汉卡德维斯生物科技有限公司(以下简称“卡德维斯”)宣布,其自主研发的一类创新注射剂新药KDTV001的临床试验申请获中国国家药品监督管理局批准,取得全球首创结果。同时,该药于9月26日向美国食品药品监督管理局(FDA)提交临床试验申请,进入审评阶段。 KDTV001注射液在中国获批,是主动免疫治疗的生物药。最初将进行I期临床试验,以评估注射液在患有HPV 16/18/52阳性的高级别宫颈鳞状上皮内病变的成年女性患者中的安全性、耐受性、免疫原性和初步疗效。宫颈癌是一种恶性肿瘤,严重威胁全世界女性的健康,在日本发病率居第二位。这是 e预计到2020年,全球将有604,000名女性被诊断患有宫颈癌,约342,000名女性将死于这种癌症。世界卫生组织的加速消除宫颈癌全球战略指出,90% 被诊断患有宫颈癌的女性需要治疗。持续的高危人乳头瘤病毒(HPV)感染是宫颈癌和癌前病变的主要原因。特别值得关注的是最重要的癌前阶段、宫颈高级鳞状上皮内病变 (CIN2/3) 的临床风险。权威研究数据证实,未经治疗的CIN3患者中有30%~50%会在30年内发展为宫颈癌,且随着病程延长,这种风险可能进一步累积,凸显了早期有效干预宫颈重度鳞状上皮内病变的紧迫性。 KDTV001注射液主要针对晚期实体瘤、肿瘤等适应症。早期非侵袭性肿瘤,以及HPV感染引起的宫颈高级鳞状上皮内病变。该注射液由凯德维斯旗下武汉凯德金果生物科技有限公司研发,负责创新生物医药产品的研发。卡德威斯是与华中科技大学同济医学院附属同济医院及马丁学术成员团队合作创立的一家新型国家专业“小巨人”公司。公司已申请专利51项,其中发明专利48项,实用新型专利3项。此外,我们还建立了完整的活病毒载体基因治疗药物平台,从研发到生产的高效率,保证了药品的安全性、有效性和质量可控。 2023年,公司基因治疗药物KD01重组溶瘤病毒获得国家药品监督管理局批准并进入I期临床试验。
湖北日报讯(记者张珍珍)10月13日,武汉卡德维斯生物科技有限公司(以下简称“卡德维斯”)宣布,其自主研发的一类创新注射剂新药KDTV001的临床试验申请获中国国家药品监督管理局批准,取得全球首创结果。同时,该药于9月26日向美国食品药品监督管理局(FDA)提交临床试验申请,进入审评阶段。 KDTV001注射液在中国获批,是主动免疫治疗的生物药。最初将进行I期临床试验,以评估注射液在患有HPV 16/18/52阳性的高级别宫颈鳞状上皮内病变的成年女性患者中的安全性、耐受性、免疫原性和初步疗效。宫颈癌是一种恶性肿瘤,严重威胁全世界女性的健康,在日本发病率居第二位。这是 e预计到2020年,全球将有604,000名女性被诊断患有宫颈癌,约342,000名女性将死于这种癌症。世界卫生组织的加速消除宫颈癌全球战略指出,90% 被诊断患有宫颈癌的女性需要治疗。持续的高危人乳头瘤病毒(HPV)感染是宫颈癌和癌前病变的主要原因。特别值得关注的是最重要的癌前阶段、宫颈高级鳞状上皮内病变 (CIN2/3) 的临床风险。权威研究数据证实,未经治疗的CIN3患者中有30%~50%会在30年内发展为宫颈癌,且随着病程延长,这种风险可能进一步累积,凸显了早期有效干预宫颈重度鳞状上皮内病变的紧迫性。 KDTV001注射液主要针对晚期实体瘤、肿瘤等适应症。早期非侵袭性肿瘤,以及HPV感染引起的宫颈高级鳞状上皮内病变。该注射液由凯德维斯旗下武汉凯德金果生物科技有限公司研发,负责创新生物医药产品的研发。卡德威斯是与华中科技大学同济医学院附属同济医院及马丁学术成员团队合作创立的一家新型国家专业“小巨人”公司。公司已申请专利51项,其中发明专利48项,实用新型专利3项。此外,我们还建立了完整的活病毒载体基因治疗药物平台,从研发到生产的高效率,保证了药品的安全性、有效性和质量可控。 2023年,公司基因治疗药物KD01重组溶瘤病毒获得国家药品监督管理局批准并进入I期临床试验。